USB-PIOの紹介: 生葉への光の影響の測定
I– はじめに
SECMの導入の直後に、植物を調査するためにSECMを使用することについてLee達によって実証が行われました。[1]数年後に、SECMは生きた植物を調査するのに使用できることが明らかになりました[2]。これらの作業以降、SECMは数多くの植物の調査に使用されてきており[3]、特に植物の気孔活動の調査に有効なことが証明されています[2-4]。
植物の気孔(図1)は光合成のためのCO2 の進入、O2およびH2O副産物の損失を調節するのに役立ちます。気孔の開閉に影響する多くの要因の一つは光とその強度です。気孔自体は周囲の孔辺細胞によって開閉されます。気孔が開いている時、孔辺細胞は膨らんでおり、周囲のエリアよりも高いトポグラフィとなっています。孔辺細胞は気孔が閉じると緩み、そのトポグラフィは膨らんだ状態の時よりも低くなります[5]。これはSECMを使用して生きた植物の葉への光の影響を調査する時に、2つの異なる影響が検出できることを意味します。(1) O2濃度の変化による電流の変化。(2) 気孔の周囲のトポロジの変化による電流の変化。
本書はSECMを使用して青色LED (Light Emitting Diode: 発光ダイオード)のオン/オフの切り替えが生きた植物の葉に与える影響を調査します。
CO2
H2O+O2
孔辺細胞
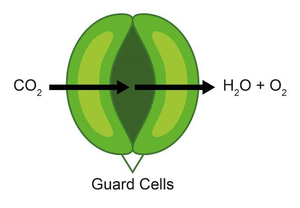
図1: 植物の気孔の概略図。孔辺細胞は気孔を開閉し、CO2を進入させてH2OおよびO2を放出させる
この作業のために、一般的な室内用鉢植え植物である生きたオリヅルラン (Chlorophytum comosum variegata)の葉が測定されました。LEDのオン/オフ切り替えのために、USB-PIO (Universal Serial Bus – Parallel Input Output: ユニバーサル・シリアル・バス – 並列入出力)アクセサリ(製品番号: U-USB-PIO)が使用されました。USB-PIOを使用することで、一連の実験およびモジュラ・マップ実験の間に青色LEDのオン/オフ切り替えの影響を調査するのが可能になりました。
II – USB-PIOの使用
USB-PIOを図2に示します。これは走査型電気化学ワークステーション・ソフトウェア(M470)内から低電圧ランプやLEDのような外部装置のオン/オフ切り替えをするのに設計された走査型電気化学ワークステーションのオプション・アクセサリです。それをPCに接続するUSBによって電力が供給されます。DB25メス型ピンがあり、ユーザ・ケーブル、または提供されているケーブルおよびブレイクアウトPCBとのインターフェースを可能にします。USB-PIOは最大4つの異なるチャネルを個別にまたは一括して制御するのに使用することができます。

図2: 供給されたブレイクアウトPCBに接続されているUSB-PIO。この画像は見本でしかなく、ユーザはブレイクアウトPCBが実験のセットアップのために正しく収納されていることを確認する。
実験でのUSB-PIOの制御は以下の3つの方法のうちの1つで行うことができます。
フランス、38640 クレ、ヨーロッパ通り1、Bio-Logic Science Instruments
電話: +33 476 98 68 31 – Fax: +33 476 98 69 09 www.bio-logic.info
1.実験がオープンでない場合、USB-PIOは[Experiment]ドロップダウンメニューの[Parallel I/O]オプションへ/から書き込むことができます(図3a)。
2.実験シーケンスを書き込むことができ、USB-PIOの出力を異なる実験の間で切り替えることが可能です(図3b)。これによって、ユーザが順序付けられるどんな実験にもUSB-PIOを使用することができます。
3.dc-SECMベースのモジュラ・マップ実験を行うことができます。ここではUSB-PIO出力を切り替えることができ、次に移る前に個々のx-y点で一連のイベントの間に入力を読み込むことができます。これは[Modular]タブの[Sequence of Events]メニューにプログラミングされています。
モジュラ・マップ実験でのUSB-PIOの使用は、USB-PIOでの各変化の間で全体的なエリアスキャン実験を行うことよりもユーザが個々の点でUSB-PIOへ/からの書き込み/読み込みができるという点でシーケンス化された実験での使用とは異なります。
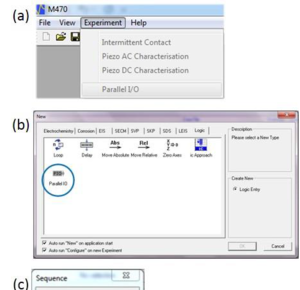
図3: USB-PIOは走査式電気化学ワークステーション・ソフトウェア(M470)で3つの方法のうちの1つで制御が可能。
(a) [Experiment]ドロップダウン・メニューからの独立した実験。
(b) 実験シーケンスの[Logic]ステップ。
(c) MMEの間の一連のイベントの一部
表I: シーケンスでのUSB-PIOの使用とMMEでの使用の比較
| シーケンスでのUSB-PIOの使用 | MMEでのUSB-PIOの使用 |
|---|---|
| 書き込みのみ | 書き込みおよび読み込み |
| シーケンスに入れることができるいかなる実験でも使用できる | ステップスキャンdc- SECMタイプの実験でしか使用できない |
| 実験の間、USB-PIOチャネルでの変化が適用される | 個々のx-y点でUSB-PIOチャネルでの変化が適用される |
| 単なるUSB-PIOの影響以上のものが見られることがある(熱ドリフトなど) | 期間が短いとUSB-PIOの影響のみが見られる |
これによってユーザは測定された変化が全エリアスキャン測定期間で起こることがあるドリフトやファウリングではなくUSB-PIOで制御している装置によるものであることを確信することができます。USB-PIOのシーケンスでの使用とMMEでの使用は表Iで比較されています。
本書はシーケンス化されたSECM実験およびMME実験でのUSB-PIOの使用を実証することが目的です。
III – 方法
ビーカがMicro TriCellの底板に取り付けられ、Micro TriCellベースの脚で水平にできるようにしました。オリヅルランの葉が茎についたままの状態でビーカに置かれ、気孔が最大密度になっている葉の裏側が上に向けられました[5]。
葉はシリコン・チューブ・リングで定位置に保持されました。セットアップの概略図を図4に示します。
M470
XYZコントローラおよび電位
RE
CE
WE
X
Y
Z
PC
X
Y
Z
スキャンヘッド
USB PIOおよびブレイクアウトPCB
NC
NO
COM
R270Ω
9V
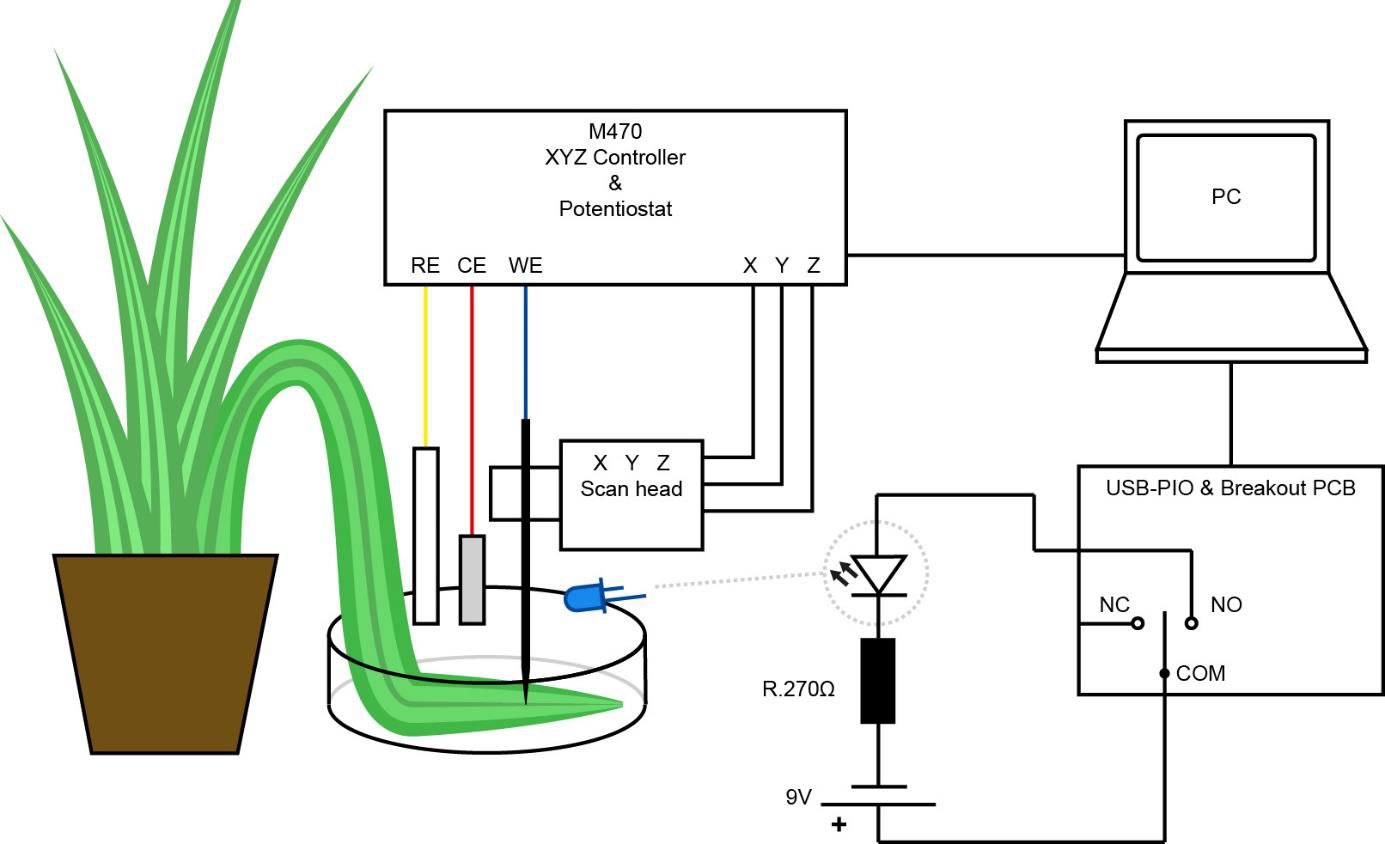
図4: USB-PIOを使用した青色LEDのオン/オフ切り替えの影響を調べるオリヅルランの葉の実験の概略図
SECM測定が直径10μmのPt UMEプローブを使用して0.1 x 10-3 mol L-1 KClで行われました。電解液内のK+の存在は気孔が閉じるのに影響しますが、ここでは低濃度が使用され、光がなお、その活性に影響することを意味します[6]。
SCE参考電極およびPtシート対電極が使用されました。関連するレドックス反応は植物の気孔から解放されるO2の減少だったため、Pt UMEは-0.75 V vs. SCEでバイアスをかけられていました。測定中のプローブの高さは、周辺光の中の植物へのアプローチカーブによって決定されました。
青色ダイオード光を使用した測定を行う前に、まず周辺光でのエリアスキャンが行われ、エリアの測定への適合性が決定されました。青色LEDの影響を決定するのに行われる測定のために、スキャンヘッドが不透明なカバーの下に置かれ、実験に影響する周辺光がないようにしました。
USB-PIOを使用して2つの異なるタイプの実験が行われました。どちらのケースでもUSB-PIOを使用して青色ダイオード(λpeak = 465nm)のオン/オフの切り替えをし、葉を照らしました。LEDは出力1のNCおよびCOMでUSB-PIOに接続されました。このようにLEDを接続すると、実験でチャネル1に書き込みが行われるとLEDがオンになり、チャネル1への書き込みが停止するとLEDがオフになります。望ましい場合は、ユーザはNCの代わりに出力1のNOに接続することもできます。
この場合、チャネル1に書き込まれるとLEDはオフになり、実験でチャネル1への書き込みが行われない時は常にオンになります。同じ前提がすべての出力チャネルに適用されます。最初の実験タイプで、シーケンスはUSB-PIOがLEDを10分間オンにし、SECMエリアスキャンの間オンのままにするように設定されました。このスキャンの終了後、USB-PIOはLEDをオフにしました。
次のSECMエリアスキャンを行うまで、LEDがオフにされたままの10分間の待ち時間がありました。どちらのスキャンも300μm x 300μmのエリアに対してスイープスキャンモードで行われました。データは3μmの間隔で収集されました。2番目の実験タイプでは、USB-PIOが6ステップ・モジュラ・マップ実験の一部として使用され、オリヅルランが3時間暗い場所に置かれた後、実験が行われました。
モジュラ・マップ実験のシーケンスのステップは以下の通りでした。
1.USB-PIOがLEDをオンにしました。
2.プローブが3.000秒間、0V vs. OCPで維持されました。
3.プローブが3.000秒間、-0.75Vでバイアスがかけられました。2.900秒でデータが収集され0.001秒で平均化されました (データ転送速度1000Hz)。
4.USB-PIOがLEDをオフにしました。
5.プローブが3.000秒間、0 V vs. OCPで維持されました。
6.プローブが3.000秒間、-0.75Vでバイアスがかけられました。2.900秒でデータが収集され0.001秒で平均化されました(データ転送速度1000Hz)。
各シーケンスの後、プローブは次のx-y点に移動し、シーケンスを繰り返しました。これは6μmステップで300μm x 300μmのエリアに対して行われました。これで2つの補完エリアマップが得られ、1つはイベントの各シーケンスのステップ3の間に収集されたデータから構成され、もう1つはイベントの各シーケンスのステップ6の間に収集されたデータから構成されていました。
M470またはGwyddion[7]を使用して最終2Dプロットの計算が行われました。3DIsoPlotが、得られた2Dエリアマップを3Dマップに変換するのに使用されました。
IV – 結果
IV - 1 シーケンスでのUSB-PIOの使用
USB-PIOは最初、エリアスキャン実験の間に青色LEDをオフに対してオンにする影響を決定するのに使用されました。結果は図5で見られます。この図で高電流のエリアは、気孔が開いてO2濃度が高まったことによるものです。
気孔の周囲の低電流エリアは、緩くなると葉の残りの部分よりも高くなる孔辺細胞によるものです。LEDがオンの状態で行ったスキャンからLEDがオフの状態で行ったスキャンに行くと、気孔で測定された電流が多かれ少なかれ減少するのがわかります。
|/nA
x位置/μm
y位置/μm
|/nA
x位置/μm
y位置/μm
|/nA
x位置/μm
y位置/μm
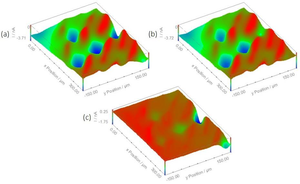
図5: LEDがオンおよびオフの状態で行った一連のSECM測定から得られたエリアマップ。
(a) USB-PIOによるエリアスキャンの間、青色LEDがオン。
(b) USB-PIOによるエリアスキャンの間、青色LEDがオフ。
(c) マップ(a)からマップ (b)を引いた結果
|/nA
x位置/μm
y位置/μm
|/nA
x位置/μm
y位置/μm
|/nA
x位置/μm
y位置/μm
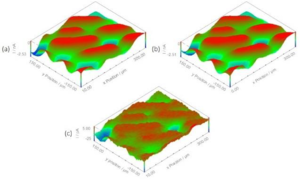
図6: 青色LEDをオン/オフに切り替えるモジュラ・マップ実験でUSB-PIOを使用して得たエリアマップ。
(a) LEDがオンの状態でモジュラ・マップ実験のステップ3の間に測定。
(b) LEDがオンの状態でモジュラ・マップ実験のステップ6の間に測定。
(c) マップ(a)からマップ (b)を引いた結果
これは特に図5cの3Dマップで顕著ですが、このマップはLEDをオンにした状態で測定したマップからLEDをオフにした状態で測定したマップを引いたものです。
特に目立つのはマップの中央上部の気孔の変化で、電流がほぼ50%減少しています。LEDがオフの状態で行った測定による気孔の上の電流の減少は、暗い場所で気孔が閉じてO2濃度が低下したことと直接関連します。
図5cはまた、気孔の周囲の孔辺細胞の上で電流が正になることも示していますが、LEDがオンの時に電流が低くなることを暗示しています。これはLEDがオンの時に緩んだ孔辺細胞によってトポグラフィが増加することを示します。
IV - 2 モジュラ・マップ実験でのUSB-PIOの使用
青色LEDのオン/オフがオリヅルランから放出されたO2に与える影響は、モジュラ・マップ実験でUSB-PIOを使用することでも調査されました。この実験で作成されたエリアマップは図6に示されています。その最初の状態ではLEDがオンの状態で行われた実験とオフの状態で行われた実験での違いを認識するのは困難です。
これはあり得ることです。植物の気孔が完全に開いた後、開口部で最初の急激な減少があるとはいえ[6]、完全に閉じるまでに何時間もかかることがあるからです。このため、気孔の開閉の大きな変化が各x-y点の一連のイベントのタイムスケールで起こる可能性は低くなっています。
しかし、LEDがオフの状態で測定されたマップをLEDがオンの状態で測定されたマップから引くと、この変化の影響を十分に見ることができます(図6c)。この図は、青色LEDのオン/オフ切り替えがこの短い時間でもオリヅルランの葉に影響を与えることを示しています。
V – 結論
SECMを使用してオリヅルランの気孔の開閉に与える影響を調べるために、USB-PIOを使用して青色LED光をオン/オフにしました。
どちらの場合もLEDがオン/オフに切り替えられた時、葉の気孔と孔辺細胞にはっきりした差異がありました。
LEDをオフにした時の影響は、モジュラ・マップ実験よりも長い期間のシーケンス化実験でのほうが劇的です。
VI – 謝辞
図1および4のグラフ表示についてIan Tindle氏に感謝いたします。
参考文献
- C. Lee, J. Kwak, A. J. Bard, Proceedings of the National Academy of Science USA 87, 5 (1990) 1740-1743
- M. Tsionsky, Z. G. Cardon, A. J Bard, R. B. Jackson, Plant Physiology 113, 3 (1997) 895- 901
- J. Mauzeroll, S. B. Schougaard, in : A. J. Bard, M. V. Mirkin (Ed.), Scanning Electrochemical Microscopy, 2nd Ed., CRC Press, Boca Raton (2012) 379.
- R. Zhu, S. M. Macfie, Z. Ding, Journal of Experimental Botany, 56, 421 (2005) 2831- 2838
- T. Lawson, New Phytologist, 181, 1 (2009) 13-34
- G. D. Humble, T. C. Hsiao, Plant Physiology, 44, 2 (1969) 230-234
- Gwyddionデータ分析ソフトウェア
gwyddion.net

SECM 走査型電気化学顕微鏡の製品情報はこちら >>
電気化学測定装置のお取り扱いページへ
お問い合わせ
株式会社東陽テクニカ 理化学計測部
